[Endostory #10] Lịch sử hình thành và phát triển ESD – Từ cắt polyp tới “chuẩn mực EN-BLOC”
“Nếu muốn đi xa, hãy đứng trên vai những người khổng lồ” – câu nói này dường như đúng hơn bao giờ hết khi nhìn lại hành trình của kỹ thuật bóc tách dưới niêm mạc Endoscopic Submucosal Dissection (ESD). Những ca ESD tinh vi mà chúng ta có thể thực hiện hôm nay chính là kết quả của hàng chục năm tìm tòi, sáng tạo và bền bỉ cải tiến của thế hệ các nhà nghiên cứu y khoa.
Bước khởi đầu: Nhiệm vụ cắt toàn bộ tổn thương
Hành trình của ESD bắt đầu từ những năm 1960, khi kỹ thuật cắt polyp qua nội soi lần đầu tiên được giới thiệu [1,2]. Từ mốc khởi đầu này, các nhà nghiên cứu không ngừng tìm kiếm giải pháp loại bỏ được các mẫu tổn thương lớn hơn.
Đến khoảng những năm 1980 tới đầu 1990, tại Nhật Bản, một loạt biến thể cắt niêm mạc qua nội soi Endoscopic Mucosal Resection (EMR) ra đời như là lựa chọn điều trị xâm lấn tối thiểu cho ung thư dạ dày giai đoạn sớm với tổn thương kích thước nhỏ. Những kỹ thuật này có thể kể tới bao gồm: sinh thiết dải [3], cắt niêm mạc qua nội soi bằng tiêm dung dịch muối sinh lý tại chỗ (ERHSE) [4,5], thòng lọng đôi (EDSP) [6], và EMR với đầu gắn cap [7,8]. Những cải tiến này không chỉ nâng cao độ an toàn và tính tin cậy của can thiệp nội soi, mà còn thúc đẩy sự chấp nhận EMR trên phạm vi quốc tế.
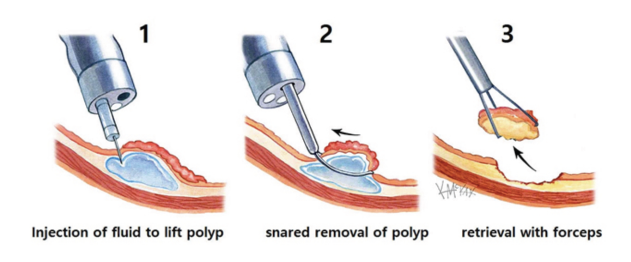
Tuy nhiên, giai đoạn trước ESD, các kỹ thuật ER vẫn bị giới hạn bởi kích thước mẫu có thể cắt bỏ, vốn phụ thuộc vào đường kính snare hoặc cap. Chỉ định ER lúc đó chủ yếu dành cho tổn thương dưới 2 cm có khả năng cắt nguyên khối. Ngay cả với tổn thương nhỏ, tỷ lệ cắt bỏ toàn bộ bằng EMR cũng chưa tới 70%, và cắt không hoàn toàn hoặc cắt từng phần đều làm tăng nguy cơ tái phát tại chỗ [9–11].
ESD được phát triển để vượt qua giới hạn này. Với kỹ thuật phẫu tích tỉ mỉ dưới niêm mạc, ESD cho phép cắt bỏ en-bloc– loại bỏ toàn bộ tổn thương kèm diện cắt bên và diện cắt sâu an toàn. Cách tiếp cận này tôn trọng nguyên tắc phẫu thuật, cách ly tổn thương dưới hình ảnh nội soi trực tiếp, cung cấp mẫu bệnh phẩm nguyên khối cho đánh giá mô học chính xác và tối ưu hóa khả năng triệt căn so với cắt từng phần.
Nhờ những ưu thế rõ rệt, ESD nhanh chóng được ứng dụng cho mọi vị trí đường tiêu hóa. Từ năm 2006, bảo hiểm y tế quốc gia Nhật Bản đã chấp chi trả cho tổn thương dạ dày–tá tràng, mở rộng cho thực quản năm 2008, và cuối cùng là đại trực tràng năm 2012.
Hàng loạt nghiên cứu, đặc biệt từ Đông Á, đã chứng minh ESD giúp tăng tỷ lệ R0 và giảm tái phát tại chỗ so với các kỹ thuật can thiệp nội soi khác [5,12–15].
Tầm cao mới của ESD: Sức mạnh của việc cải tiến không ngừng
Kỹ thuật ESD được đặc trưng bởi hai dạng chính: cắt vòng niêm mạc quanh chu vi tổn thương và phẫu tích lớp dưới niêm mạc.
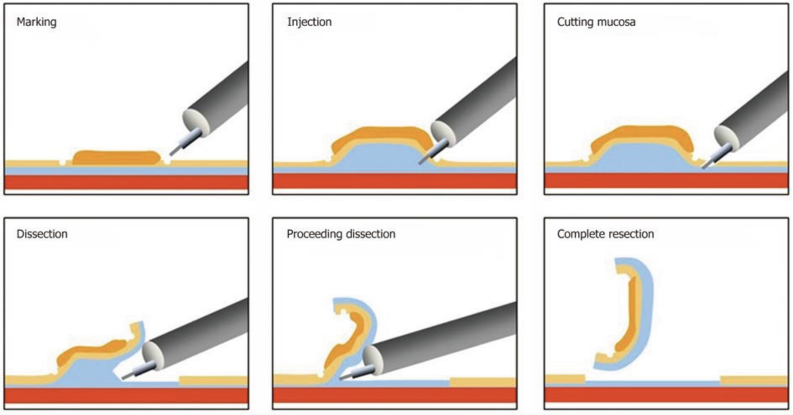
Ý tưởng rạch vòng niêm mạc để giữ nguyên vẹn diện cắt bên vốn đã xuất hiện từ thời EMR – cụ thể là kỹ thuật ERHSE, nơi việc cắt bỏ mô được hỗ trợ bằng kìm kẹp (grasping forcep) và ống soi hai kênh, tương tự như sinh thiết dải. Ban đầu, đường rạch niêm mạc được thực hiện bằng dao kim sau khi tiêm dung dịch muối sinh lý. Nhưng với đầu cắt thô sơ, dao kim dễ gây chảy máu nghiêm trọng hoặc thủng, khiến kỹ thuật này chưa được chấp nhận rộng rãi.
Bước ngoặt xảy ra khi các loại dao ESD chuyên dụng ra đời, giúp can thiệp tinh vi và an toàn hơn. Có thể chia chúng thành hai nhóm chính:
- Dao đầu tù (blunt tip) – Tiêu biểu là dao IT (Insulation-Tipped Knife) do Hosokawa và cộng sự phát triển [16–18]. Với đầu bán cầu bằng sứ, dao IT vừa đóng vai trò bảo vệ tránh cắt quá sâu, vừa giúp kiểm soát độ di động của lưỡi cắt, duy trì tốc độ phẫu tích ổn định.
- Dao đầu nhọn (cutting tip) – Cho phép phát dòng điện đa hướng từ cả đầu và cạnh lưỡi, mang lại sự linh hoạt cao nhưng đòi hỏi quan sát và thao tác cẩn trọng để đảm bảo an toàn. Nhiều loại dao đầu nhọn có cấu tạo dây cắt mảnh, ngắn, kết hợp vỏ ngoài cách điện và phần chặn ở đầu để kiểm soát độ sâu cắt, giảm nguy cơ tổn thương mô sâu. Ví dụ: Hook knife, Flex knife, Dual knife (của Olympus), Hybrid knife (của ERBE).

Cùng với dao, nguồn cắt và chế độ dòng điện là yếu tố quan trọng quyết định thành công. Sự xuất hiện của chế độ EndoCut trong nguồn cắt đốt ERBE đã mở ra khả năng điều chỉnh tự động cường độ và đặc tính dòng cắt – đông tùy theo giai đoạn thủ thuật, loại dao, và mô đích. Chế độ cắt (cutting mode) giúp bóc tách nhanh, chính xác; trong khi chế độ dòng pha trộn (blended mode) tăng độ an toàn khi phẫu tích các mô dưới niêm mạc giàu mạch máu. Hầu hết các trường hợp chảy máu xảy ra trong quá trình ESD có thể được kiểm soát tức thì bằng kẹp cầm máu (hemostatic forcep).
Việc tạo ra một lớp đệm bằng chất lỏng dưới niêm mạc (submucosal fluid cushion – SFC) cũng là một biện pháp tiện lợi để tránh làm tổn thương sâu vào lớp cơ trong quá trình can thiệp, tăng tính an toàn cho ca ESD. Với EMR nhanh sử dụng thòng, tiêm nước muối sinh lý là đủ; nhưng với các ca ESD kéo dài, sẽ cần tới loại dung dịch ổn định hơn để bảo vệ lớp cơ. Nhiều loại đã được thử nghiệm, trong đó nổi bật là hyaluronic acid (HA) – được Yamamoto và cộng sự giới thiệu [24–26] và sau đó được Bộ Y tế, Lao động và Phúc lợi Nhật Bản phê duyệt dưới dạng thuốc tiêm 0,4% cho ESD (MUCOUP, Johnson & Johnson). Bên ngoài nước Nhật, các lựa chọn khác như glycerol, dextrose, hay hydroxypropyl methylcellulose (HPMC) [27–31] cũng được áp dụng nhờ chi phí thấp và khả năng tạo đệm ổn định.
Cho tới hiện tại, các nhà nghiên cứu vẫn không ngừng tìm kiếm, cải tiến các loại dụng cụ và dung dịch tiêm [32-36] nhằm không ngừng nâng cao tính hiệu quả và sự an toàn cho kỹ thuật ESD.
Thách thức và triển vọng tương lai
Ở Nhật Bản và nhiều nước Đông Á, ESD đã trở thành lựa chọn điều trị hàng đầu cho tổn thương tiêu hóa sớm, kể cả trong chỉ định mở rộng như ung thư niêm mạc thể biệt hóa không loét, kích thước lớn. Nghiên cứu mô học nghiêm ngặt cho thấy kết quả ESD tương đương phẫu thuật trong nhóm này.
Tuy nhiên, trên thế giới, mức độ chấp nhận ESD còn khác biệt. Cụ thể như ở phương Tây, nơi tỷ lệ ung thư dạ dày sớm thấp, do vậy thiếu đi các ca lâm sàng thích hợp cho đào tạo (không giống như dữ liệu được công bố về ESD của các nước phương [12, 38, 39]), dẫn tới khó khăn trong thiết lập những kiến thức và kĩ năng cơ bản để đánh giá, phân định xác định tổn thương. Trong những ca can thiệp nội soi được dự đoán có nhiều thách thức, có thể cân nhắc các phương pháp khác, như là cắt bỏ từng phần hoặc thậm chí là tiến hành phẫu thuật.

Công nghệ mới đang mở ra triển vọng: ống nội soi điều trị với mô hình tam giác, có hai kênh dụng cụ di động hoặc các bộ điều khiển khớp nối ở đầu ống nội soi [40, 41] – cho phép kéo niêm mạc tổn thương ra khỏi mặt phẳng phẫu tích và đồng thời dùng một con dao kim bóc tách lớp cơ. Dù hiện còn cồng kềnh, các hệ thống này hứa hẹn sẽ được tối ưu hóa để ứng dụng rộng rãi trong tương lai.
Kết luận
ESD đã thay đổi cục diện điều trị tổn thương tiêu hóa sớm, mang lại khả năng cắt bỏ nguyên khối với độ chính xác và tính triệt căn cao. Trong hơn một thập kỷ qua, song hành cùng sự phát triển của dụng cụ và công nghệ, kỹ thuật này ngày càng trở nên tinh vi và an toàn hơn.
Tuy nhiên, để đạt kết quả tối ưu, bác sĩ nội soi cần được đào tạo bài bản – từ khâu chẩn đoán, chuẩn bị bệnh nhân đến quản lý sau can thiệp. Với đà tiến bộ của công nghệ, bao gồm cả phẫu thuật robot, viễn cảnh ESD trở thành chuẩn mực toàn cầu cho điều trị tổn thương sớm đường tiêu hóa là điều hoàn toàn khả thi.
Với những bác sĩ trẻ, hành trình làm chủ ESD đòi hỏi thời gian và sự kiên trì. Nhưng mỗi ca thành công không chỉ là một bước tiến nghề nghiệp, mà còn là đóng góp vào di sản của kỹ thuật này – một di sản được viết tiếp bởi chính những bàn tay và trái tim của thế hệ hôm nay.
Tài liệu tham khảo:
- 1. Niwa H. Improvement of fibrogastroscope for biopsyand application of color television and high frequentcurrents for endoscopic biopsy (in Japanese).Gastroenterol Endosc. 1968;10:315.
- Tsuneoka K, Uchida T. Fibergastroscopic polypectomywith snare method and its significance developeding our department: polyp resection and recoveryinstruments (in Japanese with English abstract).Gastroenterol Endosc. 1969;11:174–84.
- Tada M, Shimada M, Murakami F, et al. Developmentof the strip-off biopsy [in Japanese with Englishabstract]. Gastroenterol Endosc. 1984;26:833–9.
- Hirao M, Masuda K, Asanuma T, et al. Endoscopicresection of early gastric cancer and other tumors withlocal injection of hypertonic saline-epinephrine.Gastrointest Endosc. 1988;34(3):264–9.
- Kakushima N, Fujishiro M. Endoscopic submucosaldissection for gastrointestinal neoplasms. World JGastroenterol. 2008;14(19):2962–7.
- Takekoshi T, Takagi K, Fujii A, et al. Treatment of earlygastric cancer by endoscopic double snare polypectomy(EDSP). Gan No Rinsho. 1986;32(10):1185–90.
- Inoue H, Takeshita K, Hori H, et al. Endoscopicmucosal resection with a cap-fi tted panendoscope foresophagus, stomach, and colon mucosal lesions.Gastrointest Endosc. 1993;39(1):58–62.
- Inoue H, Endo M, Takeshita K, et al. A new simplifi edtechnique of endoscopic esophageal mucosal resectionusing a cap-fi tted panendoscope (EMRC). SurgEndosc. 1992;6(5):264–5.
- Gossner L. The role of endoscopic resection and ablationtherapy for early lesions. Best Pract Res ClinGastroenterol. 2006;20(5):867–76.
- Sumiyama K, Gostout CJ. Novel techniques andinstrumentation for EMR, ESD, and full-thicknessendoscopic luminal resection. Gastrointest EndoscClin N Am. 2007;17(3):471. 85, v–vi.
- Gotoda T. Endoscopic resection of early gastric cancer.Gastric Cancer.2007;10(1):1–11.
- Draganov PV, Gotoda T, Chavalitdhamrong D, et al.Techniques of endoscopic submucosal dissection:application for the Western endoscopist? GastrointestEndosc. 2013;78(5):677–88.
- Toyonaga T, Man-i M, East JE, et al. 1,635 Endoscopicsubmucosal dissection cases in the esophagus, stomach,and colorectum: complication rates and longtermoutcomes. Surg Endosc. 2013;27(3):1000–8.
- Toyonaga T, Man-i M, Chinzei R, et al. Endoscopictreatment for early stage colorectal tumors: the comparisonbetween EMR with small incision, simplifi ed ESD,and ESD using the standard fl ush knife and the balltipped fl ush knife. Acta Chir Iugosl. 2010;57(3):41–6.
- Tanabe S, Ishido K, Higuchi K, et al. Long-term outcomesof endoscopic submucosal dissection for earlygastric cancer: a retrospective comparison with conventionalendoscopic resection in a single center.Gastric Cancer. 2014;17:130.
- Ohkuwa M, Hosokawa K, Boku N, et al. New endoscopictreatment for intramucosal gastric tumorsusing an insulated-tip diathermic knife. Endoscopy.2001;33(3):221–6.
- Ono H, Kondo H, Gotoda T, et al. Endoscopic mucosalresection for treatment of early gastric cancer. Gut.2001;48(2):225–9.
- Hosokawa KYS. Recent advances in endoscopicmucosal resection for early gastric cancer [Japanese].Gan To Kagaku Ryoho. 1998;25:476–83.
- Oyama T, Tomori A, Hotta K, et al. Endoscopic submucosaldissection of early esophageal cancer. ClinGastroenterol Hepatol. 2005;3(7 Suppl 1):S67–70.
- Yahagi N, Fujishiro M, Kakushima N, et al.Endoscopic submucosal dissection for early gastriccancer using the tip of an electrosurgical snare (thintype). Dig Endosc.2004;16:34–6.
- Yahagi N, Neuhaus H, Schumacher B, et al. Comparisonof standard endoscopic submucosal dissection (ESD)versus an optimized ESD technique for the colon: ananimal study. Endoscopy. 2009;41(4):340–5.
- Toyonaga T, Man-I M, Fujita T, et al. The performanceof a novel ball-tipped Flush knife for endoscopicsubmucosal dissection: a case-control study.Aliment Pharmacol Ther. 2010;32(7):908–15.
- Neuhaus H, Wirths K, Schenk M, et al. Randomizedcontrolled study of EMR versus endoscopic submucosaldissection with a water-jet hybrid-knife of esophageallesions in a porcine model. Gastrointest Endosc.2009;70(1):112–20.
- Yamamoto H, Yahagi N, Oyama T, et al. Usefulnessand safety of 0.4% sodium hyaluronate solution as asubmucosal fluid “cushion” in endoscopic resectionfor gastric neoplasms: a prospective multicenter trial.Gastrointest Endosc. 2008;67(6):830–9.
- Yamamoto H, Yube T, Isoda N, et al. A novel methodof endoscopic mucosal resection using sodium hyaluronate.Gastrointest Endosc. 1999;50(2):251–6.
- Yamamoto H, Koiwai H, Yube T, et al. A successfulsingle-step endoscopic resection of a 40 millimeterflat-elevated tumor in the rectum: endoscopic mucosalresection using sodium hyaluronate. GastrointestEndosc. 1999;50(5):701–4.
- Fujishiro M, Yahagi N, Kashimura K, et al. Tissuedamage of different submucosal injection solutionsfor EMR. Gastrointest Endosc. 2005;62(6):933–42.
- Fujishiro M, Yahagi N, Kashimura K, et al. Comparisonof various submucosal injection solutions for maintainingmucosal elevation during endoscopic mucosalresection. Endoscopy. 2004;36(7):579–83.
- Fujishiro M, Yahagi N, Kashimura K, et al. Differentmixtures of sodium hyaluronate and their ability tocreate submucosal fl uid cushions for endoscopicmucosal resection. Endoscopy. 2004;36(7):584–9.
- Conio M, Rajan E, Sorbi D, et al. Comparative performancein the porcine esophagus of different solutionsused for submucosal injection. Gastrointest Endosc.2002;56(4):513–6.
- Feitoza AB, Gostout CJ, Burgart LJ, et al.Hydroxypropyl methylcellulose: a better submucosalfluid cushion for endoscopic mucosal resection.Gastrointest Endosc. 2003;57(1):41–7.
- Sumiyama K, Gostout CJ, Rajan E, et al. Chemicallyassisted endoscopic mechanical submucosal dissectionby using mesna. Gastrointest Endosc. 2008;67(3):534–8.
- Sumiyama K, Tajiri H, Gostout CJ, et al. Chemicallyassisted submucosal injection facilitates endoscopicsubmucosal dissection of gastric neoplasms.Endoscopy. 2010;42(8):627–32.
- Sumiyama K, Toyoizumi H, Ohya TR, et al. A doubleblind,block-randomized, placebo-controlled trial toidentify the chemical assistance effect of mesna submucosalinjection for gastric endoscopic submucosaldissection. Gastrointest Endosc. 2014;79:756.
- Chandrasekhara V, Sigmon Jr JC, Surti VC, et al. Anovel gel provides durable submucosal cushion forendoscopic mucosal resection and endoscopic submucosaldissection. Surg Endosc. 2013;27(8):3039–42.
- Khashab MA, Saxena P, Sharaiha RZ, et al. A novelsubmucosal gel permits simple and effi cient gastricendoscopic submucosal dissection. Gastroenterology.2013;144(3):505–7.
- Gotoda T, Iwasaki M, Kusano C, et al. Endoscopicresection of early gastric cancer treated by guidelineand expanded National Cancer Centre criteria. Br JSurg. 2010;97(6):868–71.
- Draganov PV, Coman RM, Gotoda T. Training forcomplex endoscopic procedures: how to incorporateendoscopic submucosal dissection skills in the West?Expert Rev Gastroenterol Hepatol. 2014;8:119.
- Schumacher B, Charton JP, Nordmann T, et al.Endoscopic submucosal dissection of early gastric neoplasiawith a water jet-assisted knife: a Western, singlecenterexperience. Gastrointest Endosc. 2012;75(6):1166–74.
- Ikeda K, Sumiyama K, Tajiri H, et al. Evaluation of anew multitasking platform for endoscopic fullthicknessresection. Gastrointest Endosc. 2011;73(1):117–22.
- Yonezawa J, Kaise M, Sumiyama K, et al. A noveldouble-channel therapeutic endoscope (“R-scope”)facilitates endoscopic submucosal dissection of superficial gastric neoplasms. Endoscopy. 2006;38(10):1011–5.
- Ho KY, Phee SJ, Shabbir A, et al. Endoscopic submucosaldissection of gastric lesions by using a Masterand Slave Transluminal Endoscopic Robot(MASTER). Gastrointest Endosc. 2010;72(3):593–9.
- Phee SJ, Reddy N, Chiu PW, et al. Robot-assistedendoscopic submucosal dissection is effective in treatingpatients with early-stage gastric neoplasia. ClinGastroenterol Hepatol. 2012;10(10):1117–21.
ENDOSTORY là chuyên mục chia sẻ ca lâm sàng nội soi tiêu hóa thực tiễn thực hiện bởi Lenus Việt Nam, hướng tới mục tiêu mang lại những thông tin hữu ích dành cho các bác sĩ nội soi. Mỗi tuần một “câu chuyện” sẽ được chọn lọc và đăng tải lên fanpage Lenus Việt Nam vào lúc 20h ngày Thứ Sáu.
Chuyên mục được cố vấn chuyên môn bởi BS. Trần Đức Cảnh – chuyên gia chẩn đoán và điều trị ung thư sớm. Không chỉ là bác sĩ trực tiếp tham gia rất nhiều những ca ESD phức tạp, bác sĩ Trần Đức Cảnh còn là người thầy đào tạo kỹ thuật ESD cho rất nhiều các bác sĩ nội soi trẻ tại Việt Nam, góp phần phổ biến rộng rãi kỹ thuật được coi là “chìa khoá vàng” trong điều trị ung thư sớm đường tiêu hoá này. Tinh thần chia sẻ để lan toả của bác sĩ chính là một phần cảm hứng cho sự ra đời của hành trình “kể chuyện nội soi” ENDOSTORY này.